Chapitres
- 01. La définition d'un ion
- 02. Les cations et les anions
- 03. Neutralité électrique de la matière
- 04. Structure électronique des ions monoatomiques
- 05. Le cristal ionique
- 06. Les échanges d'électrons via les réactions d'oxydo-réduction
- 07. L'utilisation des réactions d'oxydo-réduction via électrolyse
- 08. La solution électrolytique

La définition d'un ion

Définition: un ion est une espèce chimique monoatomique ou polyatomique électriquement chargée.
Un ion se forme à partir d'une espèce chimique qui suite à un phénomène chimique (réaction) ou un phénomène physique (frottement mécanique, rayonnement) perd ou gagne un ou plusieurs électrons.
Autre formulation
Un ion est un atome, qui à perdu ou gagné un ou plusieurs électrons ( 3 max. ). Exemple, le lithium (Li) perd un électron il devient l'ion de lithium (Li+). Un autre exemple, le fluor (F) gagne un électron, il devient l'ion de fluor (F-). Si un atome perd 2 électrons, imaginons que cette atome soit l'hydrogène (H), il devient l'ion d'hydrogène (H+2).
- Un atome (ou groupe d'atomes) qui perd un ou plusieurs électrons devient une espèce chimiquement chargée appelée ion. La charge du noyau reste inchangée.
- Un ion négatif est un atome (ou groupe d'atome) qui à gagné un ou plusieurs électrons.
- Un ion positif est un atome (ou groupe d'atome) qui à perdu un ou plusieurs électrons.
L'électron est donc l'un des composants de l'atome au même titre que les neutrons et protons. C'est une particule élémentaire que l'on note petit e et dont la charge élémentaire est de signe négatif. Ils s'organisent autour du noyau de l'atome dans ce que l'on appelle un nuage électronique.
Les électrons et leurs propriétés ont aidé à la compréhension d'une multitude de phénomènes physiques, notamment en termes de conductivité.
Les cations et les anions

On distingue sorte d'ions :
- Les ions positifs appelés cations qui se forment en perdant des électrons
Exemples: H+, Cu2+, NH4+ - Les ions négatifs appelés anions qui se forment en gagnant des électrons
Exemples: OH-, S2-, HCOO-
Neutralité électrique de la matière
A l'échelle macroscopique (échelle humaine) la matière liquide ou solide est toujours électriquement neutre ce qui implique qu'une matière ionique est toujours composée de cations et d'anions qui composent leur charge électriques. Cette neutralité permet de prévoir la proportion des cations et des anions.
Exemple:
- Du chlorure de sodium contient autant d'ions chlorure ( Cl- ) que d'ions sodium ( Na+ ) car chacun ne porte qu'une seule charge.
- Du chlorure d'aluminium comporte trois fois plus d'ions chlorure ( Cl- ) que d'ions aluminium ( Al3+ ) car il faut réunir trois ions chloure pour compenser la charge portée par un ion aluminium.
Structure électronique des ions monoatomiques
Etant donné qu'un ions se forme en perdant ou en gagnant des électrons sa structure électronique est différente de celle de l'atome de départ mais Il est possible de la déduire de la formule de l'ion :
- La formule de l'ion indique comment il s'est formé. Par exemple un exposant 2+ indique qu'il y a eu perte de deux électrons, un exposant - indique qu'il y a eu gain d'un électron.
- Il faut reprendre la structure électronique de l'atome initiale et ajouter ou retirer les électrons gagnés ou perdu de la dernière couche.
Exemple: structure électronique de l'ion Al3+
La formule Al3+ indique que l'ion aluminium s'est formé en perdant 3 électrons
La structure électronique de l'atome d'aluminium de numéro atomique 13 est ( K )2( L )8( M )3.
Si l'on retire 3 électrons de la dernière couche alors la couche M qui comportait initialement 3 électrons devient vide et il n'est plus nécessaire de l'écrire.
La configuration électronique de l'atome d'aluminium est donc ( K )2( L )8 .
Le cristal ionique

Les cristaux ioniques sont constitués d'anions et de cations tenus entre eux par l'attraction électrique. Cette attraction est responsable de la structure géométrique qu'adoptent les ions pour former un cristal. Un ion positif va s'entourer d'ions négatifs et réciproquement et de la même manière que les atomes ou molécules forment les solides, les ions forment les cristaux.
Exemple
Dans un cristal de chlorure de sodium NaCl, les ions adoptent une structure cubique où un anion est entouré de 6 cations. Un cristal ionique est toujours électriquement neutre donc il y a autant de charges positives que négatives. Par conséquent, certains cristaux possèdent plus d'anions et de cations (ou inversement).
Cohésion des cristaux ioniques
Les ions étant jointifs, la distance qui les sépare correspond à la distance entre leur centre.
La cohésion du cristal est due à l'interaction coulombienne qui correspond à la force qui lie deux ions. La valeur de cette force peut paraître faible mais elle est bien plus importante par rapport au poids de l'ion. A cette échelle, c'est la force électrique qui domine. La température de fusion des solides ioniques est assez élevée (801 °C) pour le sel, ce qui veut dire que les liaisons entre ions sont très solides.
La loi de Coulomb
Coulomb, un physicien français, a établi en 1758 que le champ doit varier comme le carré inverse de la distance entre les charges à une précision de 0,02 sur l'exposant avec l'aide d'un dispositif appelé balance de Coulomb. Cette balance est constituée d'un fil de torsion en argent sur lequel est fixé des matériaux chargés. Ainsi, la loi d'attraction entre deux charges ponctuelles notées q1 et q2 , fixes dans le référentiel défini et séparées par une distance r, se définit ainsi :
- La force est dirigée selon la droite reliant les deux charges ;
- Elle est attractive si les charges sont de signes opposée et répulsive sinon ;
- Son intensité est proportionnelle aux valeurs de q1 et q2 et varie en raison inverse du carré de la distance r.
Il est alors possible de traduire ces caractéristiques en une formule exprimant la force exercée par q1 sur q2 :

Avec :
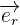 le vecteur unitaire de la droite reliant q1 et q2 qui est dirigée dans le sens 1 vers 2
le vecteur unitaire de la droite reliant q1 et q2 qui est dirigée dans le sens 1 vers 2 la permittivité diélectrique du vide
la permittivité diélectrique du vide
Ce qui peut rendre la compréhension de cette formule compliquée est la notion de force à distance. En effet, comment une charge peut savoir qu'une autre charge ponctuelle se trouve à une certaine distance d'elle et alors exercer sur force sur cette charge en fonction de la distance qui les sépare.
Dans ce cas, tout comme pour un champ gravitationnel, il peut être utile de séparer dans la loi de force ce qui dépend de la charge subissant la force et donc d'obtenir la relation suivante :

Avec :
 un champ électrique électrostatique créé à partie de la charge q1 au point où se trouve la seconde charge q2
un champ électrique électrostatique créé à partie de la charge q1 au point où se trouve la seconde charge q2
Ainsi, avec cette relation, il est plus aisé d'interpréter l’existence d'une force à distance. En effet, la charge considérée comme "source", c'est-à-dire q1, crée en tout point de l'espace un champ électrique dont la forme est donnée par la relation exprimée ci-dessus, et une charge quelconque considérée comme "test" subira l'effet de ce champ sous la forme d'une force égale au produit de cette charge par le champ électrostatique. Dans ce cas, ce champ électrostatique apparaîtra comme la force entre deux particules ponctuelles fixes par unité de charge.
Les échanges d'électrons via les réactions d'oxydo-réduction
Une réaction d'oxydoréduction, également appelée réaction redox, correspond à une réaction chimique au cours de laquelle a lieu un transfert d'électron. C'est-à-dire une réaction durant laquelle une espèce chimique dite oxydant reçoit un ou plusieurs électrons d'une autre espèce chimique dite réducteur.
Un oxydant, correspond à un ion, un corps simple ou un composé qui, lors d'une réaction d'oxydoréduction, reçoit un ou plusieurs électrons d'une autre espèce chimique. Lavoisier mettra en évidence en 1772, suite à ses manipulations du mercure, le rôle du dioxygène dans certaines réactions d'oxydoréduction. D'où le nom oxydation qui signifie "combinaison avec l'oxygène".
Un réducteur, également appelé agent de réduction, correspond à un ion, un corps simple ou un composé qui, lors d'une réaction d'oxydoréduction, cède un ou plusieurs électrons à une autre espèce chimique. Réduction quant à lui signifie "l'extraction d'un métal de son oxyde", une définition connue en métallurgie.
Développement du concept
Les réactions d'oxydo-réduction forment une grande famille puisqu'elles comprennent de nombreuses réactions chimiques. En effet, elles interviennent dans les combustions, certains dosages métallurgiques mais également la corrosion des métaux, l'électrochimie et la respiration cellulaire.
Ces réactions sont alors essentielles puisqu'elles jouent un rôle fondamental en biologie : elles permettent la transformation de l'oxygène en eau, de formule H2O, au sein des organismes vivants. Elles sont également massivement utilisées dans l'industrie humaine, notamment afin d'obtenir de la fonte à partir de différents minerais composés d'oxyde de fer grâce à une réduction, puis de fer et d'acier à partir de la fonte grâce à une réaction d'oxydation.
Ces différentes utilisations peuvent être expliquée par l'extrême mobilité de l'électron, sa légèreté mais également son omniprésence dans toutes les formes de la matière.
Les demi-équations rédox
Puisque dans une réaction d'oxydo-réduction, le réducteur s'oxyde, c'est la réaction d'oxydation et l'oxydant se réduit, c'est la réaction de réduction, l'oxydoréduction se compose donc de deux demi-réactions : une oxydation et une réduction.
Elles se présentent sous la forme suivante :
- Oxydation
- réducteur(1) = oxydant(1) + n e-
- Réduction
- oxydant(2) + n e- = réducteur(2)
- Oxydoréduction qui représente donc la "somme" de l'oxydation et de la réduction
- oxydant(2) + réducteur(1) → oxydant(1) + réducteur(2)
Notons que dans les demi-équation, les flèches n'apparaissent que si la réaction est totale, c'est à dire quand K > 10 000
Le potentiel d'oxydo-réduction
Le caractère oxydant ou réducteur d'une espèce dépend de la réaction chimique et des espèces qui interagissent entre elles. En effet, l'élément réducteur dans une réaction peut devenir l'oxydant d'une autre réaction. C'est pour cela que l'on construit une échelle de force oxydante (ou de force réductrice selon le sens donné à cette échelle) afin d'obtenir le potentiel d'oxydo-réduction se mesurant en volt.
En outre, le potentiel d'oxydo-réduction dépend du contexte chimique, notamment du pH, mais aussi du contexte physique puisque les effets de la lumière peuvent intervenir dans la nature comme ce qui est le cas avec la photosynthèse chez les plantes ou la photographie avec l'Homme.
L'utilisation des réactions d'oxydo-réduction via électrolyse

L'invention de l'électrolyse
C'est en 1800 que la toute première électrolyse a été réalisée par deux chimistes originaires de Londres, William Nicholson et Sir Anthony Carlisle. Ils réalisent une électrolyse de l'eau.
L'électrolyse met en jeu deux couples rédox. Il les fait réagir dans le sens contraire de la réaction naturelle au moyen d'un courant électrique qui apporte l'énergie nécessaire à la réaction.
Un électrolyseur est un dispositif consistant en une récipient contenant une solution ionique dans laquelle plongent deux électrodes.
Description du concept
Une électrolyse est une opération chimique dont le but est de décomposer différentes matières. Par exemple, lorsqu'une solution contient une matière, on va y ajouter un solvant afin que ses ions soient décomposables. On plonge alors ce mélange dans un bain auquel sont intégrés une anode et une cathode, faisant alors passer un courant dans le bain.
Pour être bref, afin d'obtenir une électrolyse, il faut imposer une tension électrique entre deux électrodes plongées dans une solution dite électrolytique. Cela va alors provoquer un transfert d'électron d'un oxydant vers un réducteur. L'électrolyse permet alors de provoquer des transformations dites forcées.
L'électron est donc l'un des composants de l'atome au même titre que les neutrons et protons. C'est une particule élémentaire que l'on note e et dont la charge élémentaire est de signe négatif. Ils s'organisent autour du noyau de l'atome dans ce que l'on appelle un nuage électronique. Les électrons et leurs propriétés ont aidé à la compréhension d'une multitude de phénomènes physiques, notamment en termes de conductivité.
Un oxydant, également appelé agent d'oxydation, correspond à un ion, un corps simple ou un composé qui, lors d'une réaction d'oxydoréduction, reçoit un ou plusieurs électrons d'une autre espèce chimique.
Un réducteur, également appelé agent de réduction, correspond à un ion, un corps simple ou un composé qui, lors d'une réaction d'oxydoréduction, cède un ou plusieurs électrons à une autre espèce chimique.
Ce procédé est régulièrement utilisé afin de purifier les métaux tels que le cuivre ou encore pour protéger le fer de la corrosion par électrozingage. Vous pouvez également utiliser cette technique pour embellir votre service de couvert en les argentant ou pour récupérer différentes substances telles que de l'aluminium ou du dichlore.
L'électrozingage repose sur le dépôt d'électrolyte de zinc sur le fer afin de le protéger grâce à l'obtention d'un revêtement protecteur. On dit alors du fer qu'il est électrozingué.
Dans l'industrie, afin d'affiner du cuivre brut, on utilise le cuivre en tant qu'anode dans un bain de sulfate de cuivre afin de procéder à une électrolyse. Ainsi, du cuivre pur jusqu'à un pourcentage de 99,95% se fixera sur la cathode alors que les impuretés resteront dans le bain de sulfate de cuivre.
On utilise aussi les bains électrolytiques pour le plaquage des métaux. En effet, ces procédés, connus sous les noms de dorure, argenture, nickelage, chromage, cadmiage, cuivrage, galvanoplastie ou autres consistent au recouvrement de certains objets par une couche de métal précieux comme cuivre ou de l'or par exemple.
Le fonctionnement est simple, on plonge l'objet dans un bain avec deux électrodes : une anode et une cathode. La cathode est connectée sur la pièce qui va recevoir le placage, l'anode est quant à elle reliée à du cuivre. En envoyant du courant, le cuivre va se déplacer sur l'objet. On peut réguler le placage avec différents facteurs comme la concentration ou la température qui rendront le placage plus rapide ou plus épais.
Description de l'électrode
Les électrodes se polarisent dès que le courant passe :
- L'anode est l'électrode par laquelle le courant arrive dans le système. Les électrons en sortent donc. Il y a oxydation du réducteur. Elle est reliée au pôle + du générateur.
- La cathode est l'électrode par laquelle sort le courant c'est à dire par laquelle entrent les électrons. Il s'y produit. Elle est reliée au pôle - du générateur.
Contrairement aux piles vues dans le chapitre sur le potentiel standard, le dispositif d'électrolyse n'est pas polarisé par les couples rédox mais bien par le générateur branché à ses bornes.
L'électrolyte est le milieu conducteur, la solution ionique dans laquelle baignent les anions et les cations.
Les anions de l'électrolyte migrent vers l'électrode reliée au pôle + (l’anode) et y subissent parfois une réaction d'oxydation.
Les cations de l'électrolyte migrent vers l'électrode reliée au pôle - (c’est à dire la cathode) où ils peuvent subir une réduction.
Il peut enfin y avoir éventuellement oxydation ou réduction de l'eau (voir ci-dessous les couples rédox de l'eau).
Les participants potentiels aux échanges électroniques sont donc :
- Les ions positifs ou négatifs du bain électrolytique ;
- Les molécules du solvant ;
- Les matériaux constituant les électrodes.
La solution électrolytique
On appelle solution électrolytique toute solution obtenue par la dissolution d'une substance appelée soluté dans un liquide que l'on appelle solvant. Le soluté peut être sous la forme de solide, de gaz ou de liquide et si l'eau constitue le solvant de la solution, on parle alors de solution aqueuse.
De ce fait, une solution électrolytique correspond à une solution contenant des ions. Elle est alors conductrice tout en étant électriquement neutre
Créer une solution électrolytique par dissolution de cristaux ioniques
Détermination de la masse de soluté à peser
Soit à préparer un volume V d'une solution contenant l'espèce X, de masse molaire M(X), à la concentration [X]. Il faut, en général, déterminer la masse de l'espèce X à peser.
Soit m(X) cette masse.
 or
or 
Donc  et
et 
Rappels sur la masse
En physique, la masse correspond à une grandeur physique positive et intrinsèque d'un corps.
De façon plus précise, en physique newtonienne, la masse correspond à une grandeur extensive. Cela signifie alors que la masse d'un corps formé de parties correspond à la somme des masses de ces différentes parties qui le compose.
De plus, il est essentiel de noter que la masse est une grandeur conservative. De ce fait, elle reste constante dans le cas d'un système isolé qui n'échange donc pas de matière avec son environnement.
Pour une espèce donnée, la masse m, la quantité de matière n et la masse molaire M sont liés par : 

Les propriétés
La masse peut se manifester au travers de deux propriétés fondamentales :
En effet, en mécanique statique, la masse est correspond à l'un des premières grandeurs facilement mesurables par les gens via le système de pesée puisque celle-ci permet de comparer la masse de l'objet défini avec un masse étalon connue. On appellera alors ce système la masse pesante. C'est ainsi que l'on liera la quantité de matière d'un corps à sa masse.
Tandis qu'en mécanique dynamique, la masse correspond à une grandeur qui intervient dans le principe fondamental de la dynamique comme étant la résistance de la matière au changement de vitesse. En effet, plus la masse d'un corps est importante, plus il faudra exercer une force importante pour modifier la direction ou encore sa vitesse. On appelle alors ce phénomène "masse inerte".
Ainsi, cet aspect de la masse présente un rôle essentiel dans tous les domaines de la dynamique puisqu'elle correspond à une notion présente dans grand nombre de relations de physique classique ou encore dans les calculs qui permettent de les définir. En effet, il est possible de constater une proportionnalité entre la masse inerte et la masse pesante et cela de façon totalement indépendante de la nature du matériau mis en jeu. Cela permet alors de prendre la même unité pour la masse pesante et la masse inerte et donc de pouvoir les définir comme étant égale. Ainsi, cette équivalence a permis de définir un principe d'équivalence.
L'unité
L'unité de masse est le kilogramme dans le Système international d'unités (S.I.).
Comme pour le litre il existe des sous-unités : kg ; hg ; dag ; g ; dg ; cg ; mg.
Attention à ne pas faire comme une majorité et confondre la masse avec le poids. En effet, dans le vocabulaire de la physique, le poids correspond à la force exercée par la gravité sur un corps pesant.























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Ex3
Quelle remarque pouvez vous faire à propos de la structure interne d’un ion négatif ?
j aime bien ces cours , je comprends mieux maintenant
Bonjour,
Dans l’ion ammonium, le 4 doit être écrit en indice, pas en exposant !
Cordialement,
bonjour suite à votre lecture ..dur dur je suis apiculteurs et je mais un file de cuivre sur le passage de mes abeilles a l’entrée de mes ruches je voudrais savoir si le fait que se fileetété traverser pas de l’électricité avant son installation change sa nature mangetique et moléculaire système utiliser pour réduire le nombre de parasite varro merci de m’éclairer sur se point . un api passionné
merci prof pour votre efforts
Ok merci Thomas